境外上市资讯
2025-08-06
一、新增境外上市企业
2025年7月16日-2025年7月31日,共有2家中国内地企业在中国内地以外区域*上市。
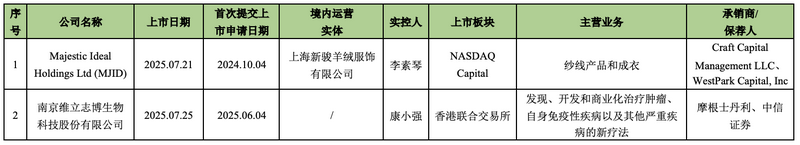
注:本处“中国内地以外区域”主要系指在中国香港联合交易所及美国纳斯达克市场,以下内容如无特殊表述均指该意,文内不予以重复注释。
二、新增境外上市申请企业
2025年7月16日-2025年7月31日,共有17家中国内地企业提交中国内地以外区域上市的申请。

三、新增境外上市备案企业
2025年7月16日-2025年7月31日,共3家内地企业通过中国证监会中国内地以外区域上市的备案。
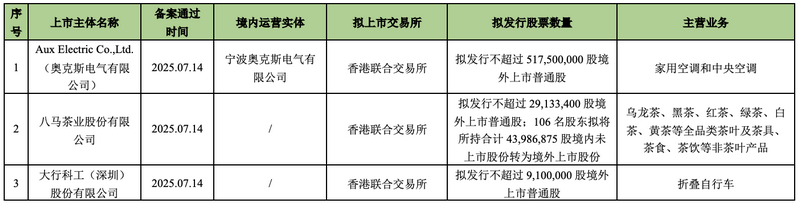
四、备案重点关注事项
2025年7月15日-2025年7月31日,中国证监会境外上市备案相关反馈问题包含如下核心关注事项:
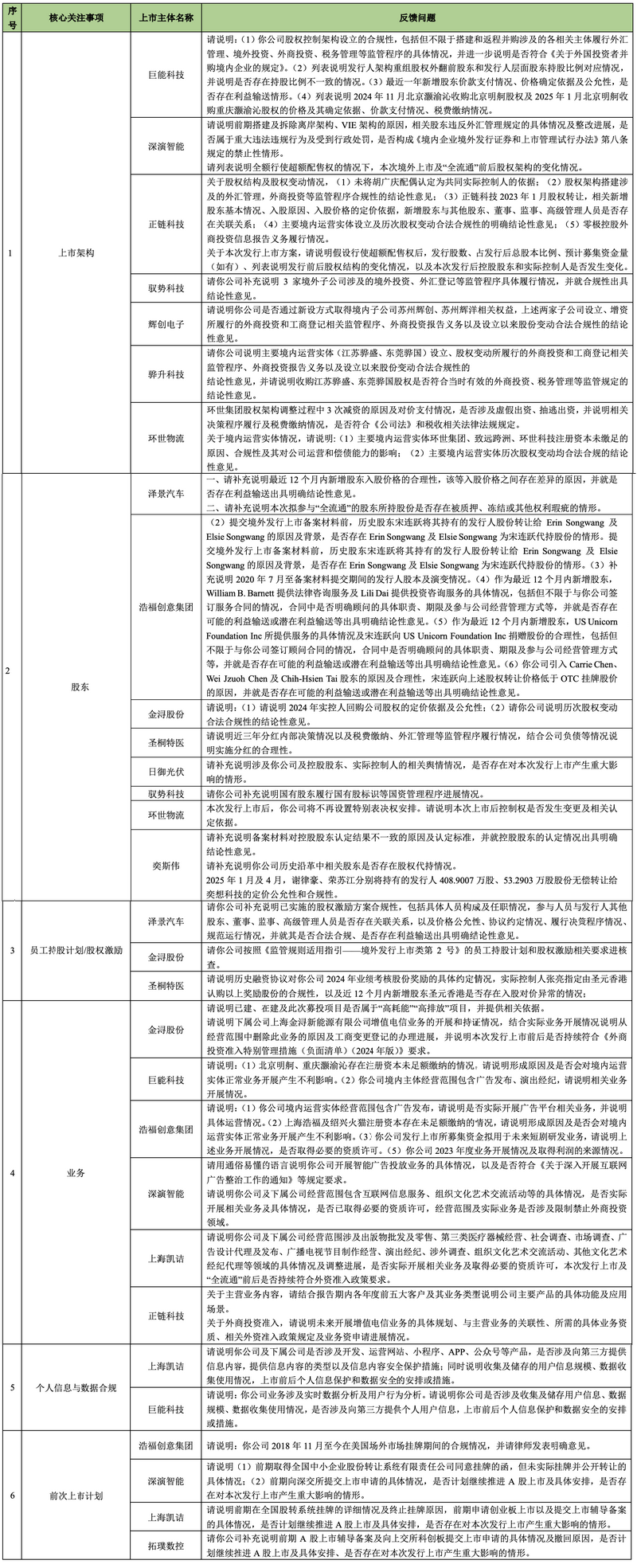
注:鉴于信息披露的口径差异,本部分内容以中国证券监督管理委员会对应信息的披露周期口径为准,故该部分统计内容存在少部分内容系为2025年7月16日至17日的反馈事项。
五、IPO市场动态
●中国资本市场学会成立大会暨第一届第一次会员代表大会圆满召开
2025年7月26日,中国资本市场学会成立大会暨第一届第一次会员代表大会在上海召开。中国证监会主席吴清出席会议并讲话,中国证监会副主席李超、国家金融与发展实验室理事长李扬、上海证券交易所理事长邱勇参加会议。来自高校科研院所、上市公司、行业机构、证监会系统以及上海市有关单位等100余名会员代表和嘉宾参加会议。
会议表决通过《中国资本市场学会章程》等重要制度,设立宏观与产业、市场稳定与风险防控、创新发展、市场微观结构、期货与衍生品、国际市场与对外开放、法治与投资者保护等7个专业委员会,选举产生学会第一届会员理事和学会负责人。中国证监会主席吴清当选学会第一届理事会会长,中国证监会副主席李超当选学会第一届理事会执行副会长。
六、热度案例分享
2025年7月25日,生物科技公司维立志博(股票代码:09887.HK)正式登陆港交所主板。维立志博成立于2012年,是一家临床阶段生物科技公司,专注于肿瘤、自身免疫性疾病及其他重大疾病新疗法的发现、开发及商业化。公司管线包括14款候选药物,其中6款已成功进入临床阶段,核心产品LBL-024已于2024年7月进入针对晚期肺外神经内分泌癌的单臂注册临床试验,是针对肺外神经内分泌癌的全球首款达到注册临床阶段的4-1BB靶向候选药物。
(一)上市基本情况
公司名称:南京维立志博生物科技股份有限公司
注册地:江苏省南京市
上市类型:H股
募资规模:每股上限定价35港元,募集资金总额约12.90亿港元
募资用途:
●研发支出:包括核心产品LBL-024的持续临床开发及监管事务、主要产品(LBL-034、LBL-033及LBL-007)的持续临床开发及监管事务、临床试验、注册申请及商业化准备等。
●生产设施建设:用于提升临床前资产、扩展管线及优化技术平台。
●提升产能:用于提升公司产能,其次用于候选药物获批销售后的商业化。
●营运资金及一般企业用途
(二)股东结构
本次IPO前,公司的主要股东包括康博士、赖博士及股份激励平台礼至合伙、引领生物有限公司及LeadsTech Limited,该等主体通过一致行动安排,共同控制公司约19.61%的投票权。维立志博成功引进正新谷资本、OrbiMed、高毅投资、真脉投资、腾讯、易方达基金、睿远基金、Sage Partners、汉康实体等基石投资者,合计认购认购金额约为6,900万美元。
(三)业务模式
1.自主药物发现与开发
维立志博专注于通过利用双特异性抗体及其他技术平台,策略性地发现及开发以T细胞为中心的免疫疗法。公司利用对T细胞免疫的见解、先进的抗体工程以及疾病生物学的充分了解,设计出可诱发强大抗肿瘤活性的分子,同时降低不良事件的风险。其核心产品LBL-024是一种PD-L1与4-1BB双特异性抗体,已进入针对多种实体瘤的注册临床阶段,展现出良好的安全性和初步疗效。此外,公司还拥有其他多款处于临床阶段的候选药物,如LBL-034(全球临床进度第二领先的靶向GPRC5D的CD3 T-cell)、LBL-033(全球仅有的两款已进入临床阶段的MUC16/CD3双特异性抗体之一)和LBL-007(在全球处于临床阶段的LAG3靶向单克隆抗体中临床进度位居前三),这些药物均针对特定的肿瘤类型,旨在通过不同的作用机制实现抗肿瘤效果。
2.合作开发与商业化
维立志博与第三方合作进行候选药物的临床开发及商业化。例如,公司曾与百济神州就LBL-007(LAG3单克隆抗体)达成授权及合作协议,在大中华区之外开发、生产及商业化该产品。尽管该合作已于2025年5月终止,维立志博重新获得了LBL-007的全球开发、生产及商业化权利,并计划进一步评估其在多种实体瘤中的治疗潜力。
3.技术平台与研发能力
维立志博建立了多个专有技术平台,包括LeadsBodyTM平台、X-body™平台(T细胞激活平台)等,该等平台具备一体化、人工智能驱动及多样化抗体工程能力,能够高效地筛选和开发具有差异化分子结构的新候选药物。公司持续投入研发,拥有由多学科背景顶尖人才组成的高级管理团队,共同推动创新药物的研发进程。此外,维立志博还拥有符合GMP标准的中试生产设施,并计划通过建设更多生产设施来满足未来商业化后的需求。
(四)行业格局
根据招股书,近年来中国肿瘤药物市场呈现持续增长,2024年收入达到人民币2582亿元,2019年至2024年的CAGR为7.2%。预计市场将大幅扩张,预计到2027年将达到人民币3434亿元,2024年至2027年的CAGR为10.0%,到2030年将进一步达到人民币5282亿元,2027年至2030年的CAGR为15.4%。
根据弗若斯特沙利文的资料,目前,抗4-1BB抗体药物正被开发用于治疗多种癌症,包括但不限于神经内分泌癌、小细胞肺癌、非小细胞肺癌、胆道癌、肝细胞癌、食管鳞状细胞癌及胃癌。该等疗法旨在通过充分利用人体的免疫系统,提供更有效、更持久且安全性良好的抗癌响应。多名参与者正开发针对肿瘤的4-1BB单克隆抗体,礼进生物的LVGN6051是唯一已进入Ⅱ期试验的候选产品,而维立志博主力产品LBL-024,截至最后可行日期为针对肺外神经内分泌癌的全球首款亦是唯一一款进入注册临床试验阶段的靶向4-1BB的免疫疗法。
注:以上全部内容均来源于公开信息汇总整理。
德恒境外上市法律服务中心(简称“境外上市中心”)隶属于德恒证券专委会,汇聚北京总部及分支机构港股、美股等境外上市领域的资深合伙人及律师,集全所优势资源,专注于境外上市全流程法律服务,包括项目承做、内核风控、资源整合、专业培训等,以卓越的执业能力护航中国企业全球资本市场布局。德恒凭借丰富的项目经验,持续为客户提供优质、精准、高效的境外上市解决方案。
本文作者:



声明:
本文由德恒律师事务所律师原创,仅代表作者本人观点,不得视为德恒律师事务所或其律师出具的正式法律意见或建议。如需转载或引用本文的任何内容,请注明出处。
